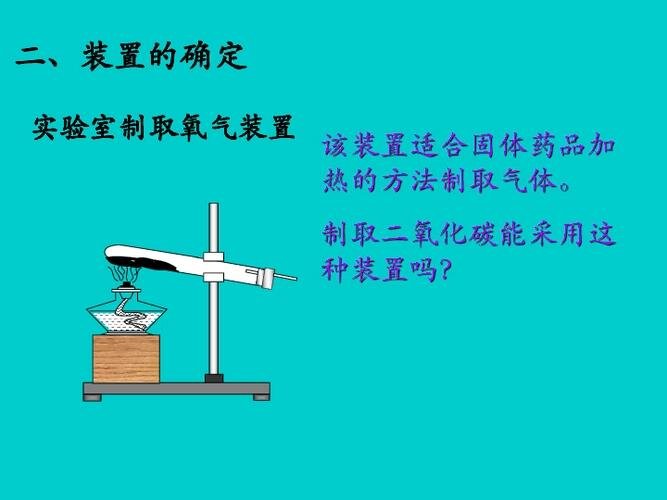
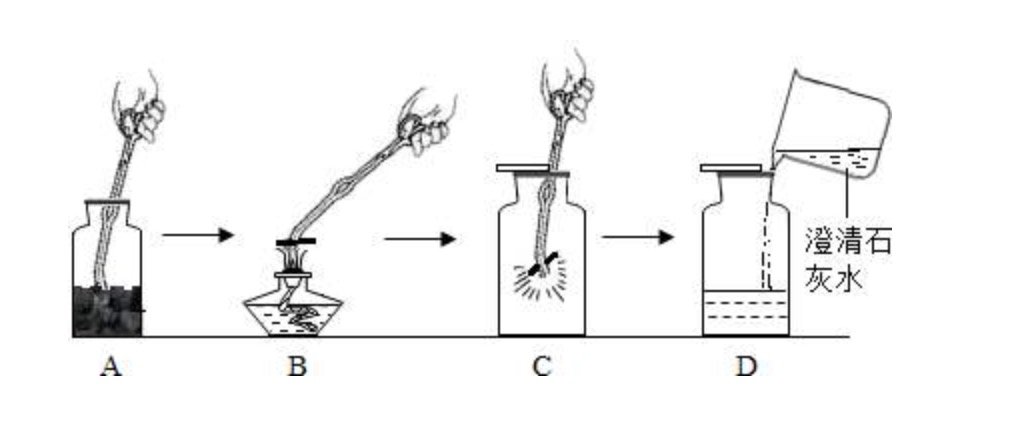
在实验室中制取二氧化碳时,可以观察到以下现象和步骤:1. 化学方程式:制取二氧化碳的化学方程式为 CaCO3 + 2HCl → CaCl2 + H2O + CO2↑。2. 反应现象:当大理石或石灰石(主要成分为碳酸钙)与稀盐酸反应时,会观察到白色固体逐渐减少,同时产生大量气泡,这些气泡中的主要气体就是二氧化碳。3. 药品选择:实验室通常使用碳酸钙(或石灰石)和稀盐酸作为反应物。4. 反应原理:该反应基于强酸制弱酸的原理,碳酸钙在稀盐酸的作用下分解生成氯化钙、水和二氧化碳。5. 实验步骤:首先检查装置的气密性,然后将碳酸钙放入反应容器中,缓慢加入稀盐酸,观察到气泡产生并收集气体。6. 收集方法:由于二氧化碳能溶于水,通常使用向上排空气法收集,或在特殊情况下使用排水法(最好将水替换为饱和碳酸氢钠溶液)。7. 验满方法:使用燃着的木条靠近集气瓶口,如果火焰熄灭,则表明二氧化碳已收集满;或观察液面变化,若液面完全处于瓶口并有气体漏出,也表明已收集满。8. 放置方法:实验室制得的二氧化碳通常会立即使用,若需放置,可在集气瓶上方的玻璃瓶中加水并盖紧,这样可以保存约10多个小时,但时间过长会导致气体不纯。请注意,制取二氧化碳时不应使用浓盐酸、硝酸或硫酸,因为这些物质可能会导致收集到的二氧化碳不纯或反应停止。